文章来源:微信公众号 医药专利
1新药定义为含中国首次上市的活性成分,含原研在国外已批准在申报进中国的化药5.1类和生物药3.1类,不含非原研仿制或进口的化药3类、生物药2类

安沐奇塔单抗的本次获批主要基于其 III 期临床研究数据 。该研究评估了两种不同剂量方案(A 组:0~12 周为 160 mg W0+80 mg Q2W,12~52 周为 80 mg Q4W;B 组:0~12 周为 160 mg Q4W,12~52 周为 160 mg Q8W)的安沐奇塔单抗注射液对中国中重度斑块状银屑病成人患者的疗效(N = 458)。
强效持久:
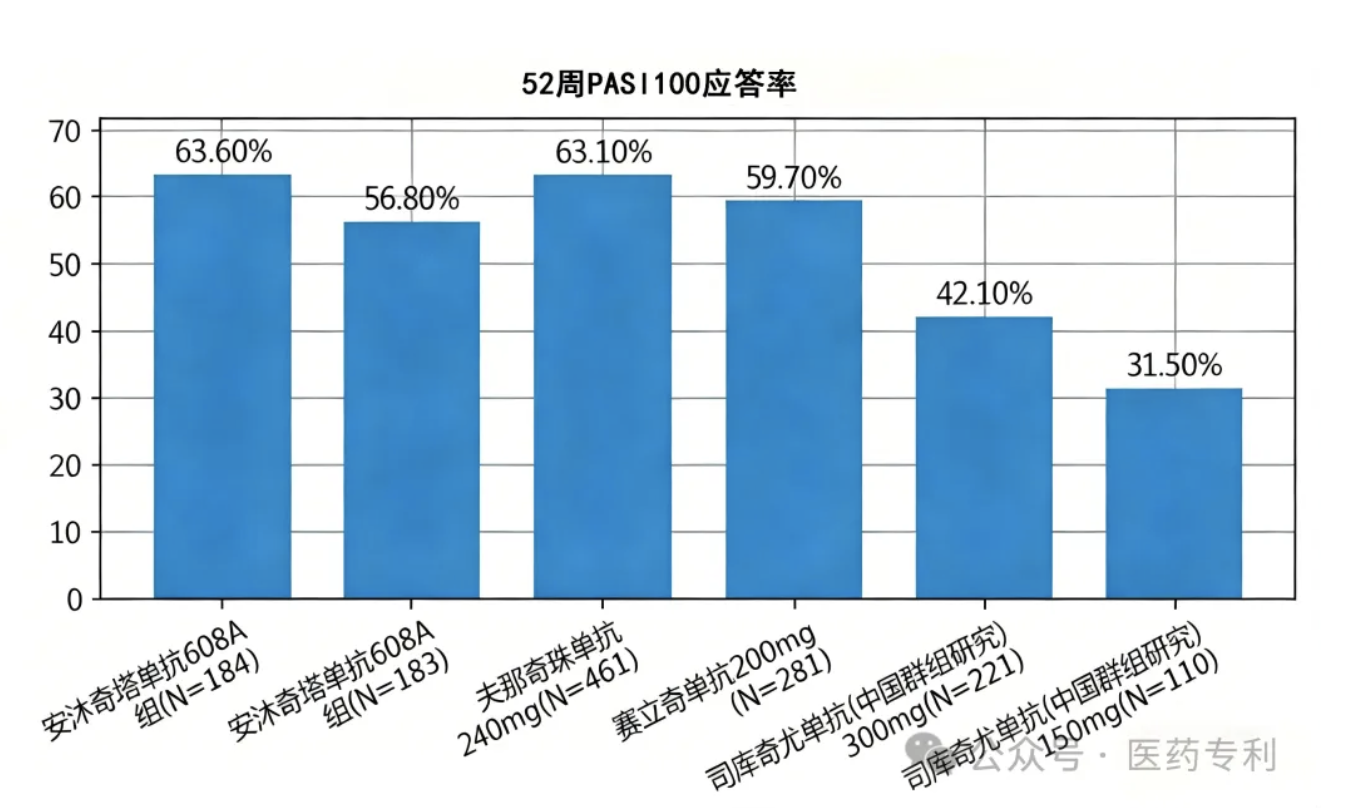
治疗第 4 周时 PASI 100 应答率达 15%,第 12 周时两个剂量组 PASI 100 应答率分别为 42.9% 和 33.9%,第 52 周时 PASI 100 应答持续改善,分别为 63.6% 和 56.8%,展现了其强效且持久的皮损完全清除能力。此外第 12 周时 PASI 75 应答率、sPGA 0/1 应答率、PASI 90 应答率均显著优于安慰剂组(P < 0.0001),且应答持续强效维持至第 52 周,两个剂量组均体现出良好的治疗持久性。
快速起效:
在第 2 周首次疗效评价时,安沐奇塔单抗组即在多项关键指标上较安慰剂组显著改善(P < 0.05),两组 PASI 评分较基线下降的变化率超 40%;第 4 周时,PASI 100 应答率达 15%;第 12 周时,A 组 PASI 100 应答率高达 42.9%。
长期耐受性良好:
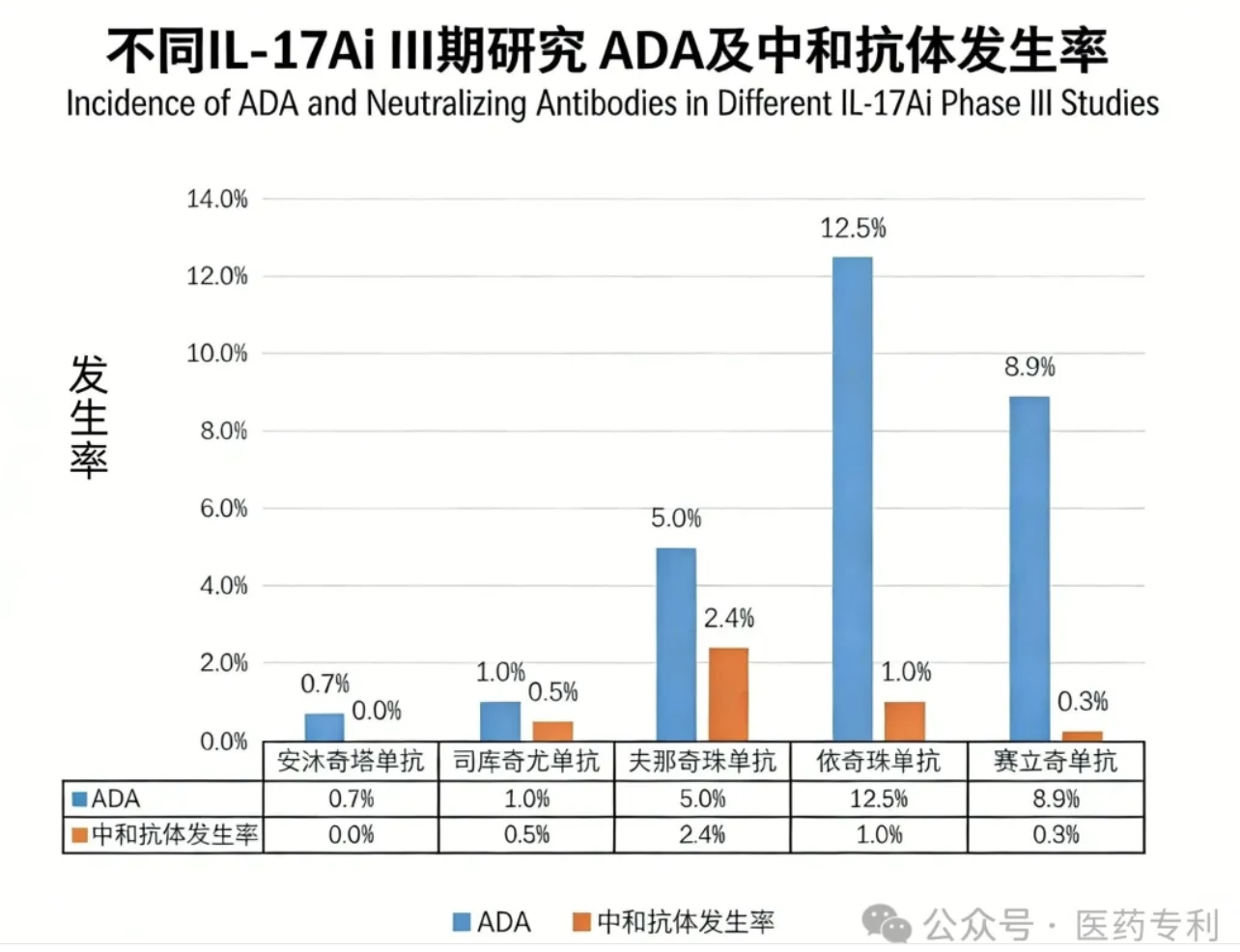
免疫原性分析显示,安沐奇塔单抗的抗药抗体(ADA)发生率低(0.7%),未检测到中和抗体。安沐奇塔单抗的低免疫原性与良好的耐受性,可降低耐药风险,为银屑病患者接受长期、稳定的治疗管理提供安全保障。其在 52 周治疗期间整体耐受性良好,药物治疗相关不良反应多数为 1~2 级,且注射部位反应发生率低(1.6%)。
安沐奇塔单抗展现出快速、深层且持久的疾病控制能力,尤其在实现 PASI 100(皮损完全清除)这一更高治疗目标方面表现突出。此外,安沐奇塔单抗的给药频率低、用药间隔长、免疫原性低、耐受性良好,为银屑病患者的长期治疗和管理提供了兼顾疗效、安全性与便捷性的用药新选择。
安沐奇塔单抗是国内目前唯一可在维持期每 8 周给药一次的 IL-17A 抑制剂。
目前国内已上市的 IL-17A 单抗均需每 4 周维持给药一次(如依奇珠单抗、司库奇尤单抗、赛立奇单抗、夫那奇珠单抗),而安沐奇塔单抗聚焦患者长期用药负担,提供了兼顾灵活性与便利性的选择,临床可根据患者情况在初始 12 周治疗后,选择在维持期每 4 周或每 8 周给药一次。
作为目前国内唯一可在维持期每 8 周给药一次的 IL-17A 抑制剂,其用药频率更低,用药间隔更长,可降低年度用药频率及治疗费用,提高患者用药便捷性和依从性,助力患者坚持长期规范治疗,为银屑病长程管理带来了全新可及选择 。
在银屑病等自身免疫疾病治疗领域,抗IL-17治疗占据的市场地位正在逐步提高。放眼全球,2025年,诺华司库奇尤单抗(Cosentyx)斩获66.68亿美元的销售额,同比增长9%。
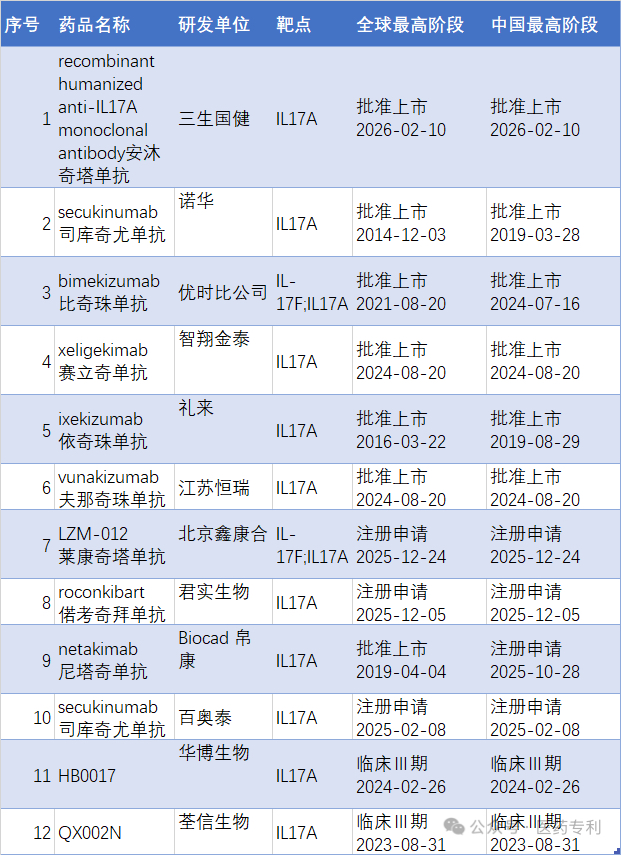
除了三生的安沐奇塔单抗,恒瑞的首个自免创新药夫那奇珠单抗和智翔金泰的首个商业化品种赛立奇单抗已率先上市。紧随其后的还有君实生物的JS005、丽珠集团的LZM012、康方生物的古莫奇单抗、荃信生物的QX002N等,均已推进至临床后期或上市申请阶段。作为自身免疫领域的兵家必争之地,抗IL-17治疗竞争的第二赛季,已迎来本土企业的陆续上场。
IL-17A药已上市6款,还有3款在注册,3款在3期临床